Chọn đến phần học sinh cần nhanh chóng thông qua mục lục bằng cách click đến phần đó
Cho nguyên tử khối: H = 1, C = 12, N = 14, O = 16, Na = 23, Mg = 24, Al = 27, S = 32, Cl = 35,5, Fe = 56, Cu = 64, Zn = 65, Ag = 108.
PHẦN I. Câu trắc nghiệm nhiều phương án lựa chọn.
Thí sinh trả lời từ câu 1 đến câu 18. Mỗi câu hỏi thí sinh chỉ chọn một phương án.
Câu 1. Kim loại Fe được điều chế trực tiếp từ $Fe_2O_3$ bằng phương pháp
A. thủy luyện
B. điện phân dung dịch
C. nhiệt luyện
D. điện phân nóng chảy
Câu 2. Khi điện phân dung dịch chất nào sau đây, tại cathode xảy ra quá trình khử nước?
A. KCl
B. $CuCl_2$
C. $AgNO_3$
D. $Fe_2(SO_4)_3$
Câu 3. Nguyên tử Na có cấu hình electron $1s^22s^22p^63s^1$. Vị trí của nguyên tố X trong bảng tuần hoàn các nguyên tố hóa học là
A. chu kì 4, nhóm IA
B. chu kì 3, nhóm IA
C. chu kì 3, nhóm IA
D. chu kì 4, nhóm VIIA
Câu 4. Phát biểu nào sau đây về liên kết kim loại là đúng?
A. Liên kết kim loại là liên kết được hình thành từ lực hút tĩnh điện giữa các cation kim loại và các electron hóa trị tự do. Vì vậy, liên kết kim loại cũng chính là liên kết ion.
B. Liên kết kim loại được hình thành do giữa các nguyên tử kim loại có sự dùng chung các electron hóa trị tự do. Vì vậy, liên kết kim loại cũng là liên kết cộng hóa trị.
C. Liên kết kim loại là liên kết được hình thành từ lực hút tĩnh điện giữa các cation kim loại và các electron hóa trị tự do trong tinh thể kim loại.
D. Liên kết kim loại là liên kết được hình thành do sự xen phủ các orbital chứa electron hóa trị tự do của các nguyên tử kim loại.
Câu 5. Nhận xét nào sau đây đúng về quá trình điện phân ở hai điện cực?
A. Cation nhường electron ở cathode
B. Anion nhận electron ở anode
C. Sự oxi hóa xảy ra ở anode
D. Sự oxi hóa xảy ra ở cathode
Câu 6. Khi điện phân nóng chảy $Al_2O_3$ với điện cực than chì, cryolite ($Na_3AlF_6$) không có tác dụng gì?
A. Hạ nhiệt độ nóng chảy của hỗn hợp
B. Tăng độ dẫn điện của hỗn hợp
C. Bảo vệ nhôm sinh ra không bị oxi hóa
D. Hạn chế điện cực bị ăn mòn
Câu 7. Mỗi thanh Mg có khối lượng 6 gam được gắn vào một đường ống dưới đất sét ẩm để chống ăn mòn cho đường ống. Khí do sẽ xuất hiện một dòng điện (gọi là dòng bảo vệ) có cường độ 0,03 A chạy giữa thanh Mg và đường ống. Điện lượng (q) của pin điện hóa được xác định bởi biểu thức q = It = $n_eF$.
Trong đó: I là cường độ dòng điện (A); t là thời gian pin hoạt động (giây); F là hằng số Faraday, F = 96845 C/mol. $n_e$ là số mol e trao đổi giữa hai điện cực. Biết hiệu suất bảo vệ đối với Mg là 50%. Khoảng thời gian đường ống có thể được bảo vệ bởi thanh Mg khỏi các tác nhân ăn mòn kim loại là
A. 25,5 năm
B. 24,5 năm
C. 20,6 năm
D. 26,8 năm
Câu 8. Dãy kim loại nào sau đây sắp xếp theo thứ tự độ dẫn điện giảm dần?
A. Au, Ag, Cu, Al
B. Ag, Au, Al, Cu
C. Cu, Al, Ag, Au
D. Ag, Cu, Au, Al
Câu 9. Phát biểu nào sau đây là đúng?
A. Ở điều kiện thường, các kim loại đều có khối lượng riêng lớn hơn khối lượng riêng của nước.
B. Tính chất hóa học đặc trung của kim loại là tính khử.
C. Các kim loại đều chỉ có một oxi hóa duy nhất trong các hợp chất.
D. Ở điều kiện thường, tất cả các kim loại đều ở trạng thái rắn.
Câu 10. Kim loại nào sau đây tác dụng với nước thu được dung dịch kiềm?
A. Al
B. K
C. Ag
D. Fe
Câu 11. Chất nào dưới đây là thành phần chính của quặng hematite?
A. Iron(II) oxide
B. Iron(III) oxide
C. Iron
D. Iron(II) sulfide
Câu 12. Chất hay hỗn hợp chất nào sau đây không phải là hợp kim?
A. Thép
B. Đồng
C. Đồng thau
D. Đồng thiếc
Câu 13. Trong nhóm IA, bán kính kim loại từ lithium đến caesium biến đổi theo xu hướng nào?
A. Tăng dần
B. Không đổi
C. Không có quy luật
D. Giảm dần
Câu 14. Để tẩy dầu mỡ đóng cặn trong dụng cụ, thiết bị và đường ống nhà bếp,…người ta thường dùng $Na_2CO_3$. Tên thương gọi của $Na_2CO_3$ là tên nào sau đây?
A. Soda
B. Baking soda
C. Xút ăn da
D. Muối ăn
Câu 15. Các kim loại kiềm có khối lượng riêng nhỏ và độ cứng thấp hơn nhiều so với các kim loại khác. Nguyên nhân là do:
(1) Tính thể có kiểu mạng lập phương tâm khối.
(2) Khối lượng nguyên tử nhỏ hơn các kim loại khác.
(3) Có lực liên kết kim loại yếu.
Chọn các ý đúng là
A. (1), (2) và (3)
B. (2) và (3)
C. (1) và (3)
D. (1) và (2)
Câu 16. Cho các phát biểu về sự ăn mòn của gang, thép trong không khí ẩm?
(a) Dạng ăn mòn hóa học là chủ yếu, do sắt dễ dàng phản ứng với oxygen trong không khí.
(b) Carbon bị khử tại cathode.
(c) Oxygen đóng vai trò là chất oxi hóa.
(d) Tại anode, Fe bị oxi hóa thành $Fe^{2+}$.
(e) Carbon đóng vai trò là cực âm (anode), sắt là cực dương (cathode) khi sự ăn mòn xảy ra.
Những phát biểu đúng là
A. (a), (b)
B. (b), (c)
C. (c), (d)
D. (d), (e)
Câu 17. Phát biểu nào sau đây đúng?
A. Kim loại kiềm có tính khử giảm dần từ Li đến Cs.
B. Dung dịch soda có môi trường acid nên được dùng để tẩy rửa dầu, mỡ trên thiết bị nhà bếp.
C. Phương pháp Solvay dùng để sản xuất soda.
D. Trong công nghiệp, người ta điều chế NaOH bằng cách cho Na tác dụng với nước.
Câu 18. Điện phân với điện cực trơ, có màng ngăn các dung dịch sau: KCl, $CuSO_4$, $AgNO_3$, $CuCl_2$, $MgCl_2$, $NiSO_4$, $ZnCl_2$. Có bao nhiều dung dịch sau điện phân có pH < 7?
A. 2
B. 3
C. 1
D. 4
PHẦN II. Câu trắc nghiệm đúng sai.
Thí sinh trả lời từ câu 1 đến câu 4. Trong mỗi ý a), b), c), d) ở mỗi câu, thí sinh chọn đúng hoặc sai.
Câu 1. Dựa vào tính chất vật lí, kim loại có nhiều ứng dụng trong đời sống.
a. Chromium thường được mạ bên ngoài một số đồ vật là do kim loại này cứng và có khả năng chống mài mòn tốt.
b. Nhôm được sử dụng nhiều trong sản xuất máy bay là do nhôm có ánh sáng kim loại phản xạ các tia cực tím từ mặt trời.
c. Bạc được dùng phổ biến làm dây dẫn điện vì là kim loại có độ dẫn điện tốt nhất.
d. Bạc được dùng để tráng gương là do bạc là kim loại dẫn nhiệt rất tốt.
Câu 2. Thực hiện thí nghiệm sau:
Bước 1: Cho dung dịch NaCl 5% vào ống thủy tinh hình chữ U như hình bên.
Bước 2: Nhúng một thanh đồng và một thanh kẽm đã làm sạch vào hai đầu của ống chữ U.
Bước 3: Nối hai thanh kim loại bằng dây dẫn.
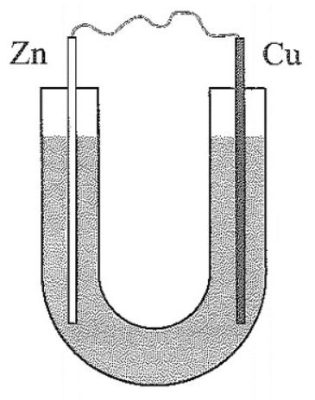
a. Hai kim loại kẽm và đồng đều bị ăn mòn.
b. Kẽm bị oxi hóa và đồng vai trò là anode.
c. $Cu^{2+}$ bị khử thành Cu bám vào thanh đồng, làm khối lượng thanh đồng tăng dần.
d. Khoảng sau bước 3, nhỏ vài giọt phenolphthalein vào dung dịch gần thanh đồng và quan sát thấy dung dịch chuyển sang màu hồng
Câu 3. Để tái chế nhôm, người ta có thể sử dụng phế liệu kim loại như vỏ của các lon, hộp chứa nước giải khát hay thực phẩm. Phế liệu này còn lẫn các tạp chất là các hợp chất hữu cơ và vô cơ (có trong nhãn, nắp in hoặc sơn trên vỏ lon, hộp). Phế liệu được cắt, bầm nhỏ rồi cho vào lò nung đến khi cháy lóng. Phần lớn các tạp chất biến thành khí lóng, nổi lên trên, được vót ra khỏi lò. Phần còn lại trong lò là nhôm tái chế ở trạng thái nóng chảy.
a. Quá trình tái chế nhôm thể hiện sự chuyển thể của nhôm lần lượt là sự nóng chảy, sự đông đặc.
b. Có thể sử dụng nhôm tái chế theo quy trình trên để tạo dụng cụ nhà bếp, y tế…
c. Giai đoạn cắt, bầm nhỏ phế liệu nhôm trước khi nung chảy: giúp giảm bớn thể tích và tiết kiệm nhiên liệu đốt nung nóng chảy.
d. Quá trình tái chế nhôm thủ công ở các làng nghề ít gây ô nhiễm môi trường.
Câu 4. Cho 3 thí nghiệm sau:
- Thí nghiệm 1: Cho mẩu sodium (Na) vào nước đã thêm vài giọt dung dịch phenolphthalein.
- Thí nghiệm 2: Cho một mẩu aluminium (Al) vào dung dịch hydrochloric acid loãng.
- Thí nghiệm 3: Cho một mẩu copper (Cu) vào dung dịch sulfuric acid đặc.
a. Các kim loại bị oxi hóa trong cả ba thí nghiệm trên.
b. Cả ba thí nghiệm trên đều tạo khí không màu, nhẹ hơn không khí.
c. Thí nghiệm 3 có sinh ra khí Z. Tỉ khối hơi của Z so với khí X thoát ra ở thí nghiệm 1 là 32.
d. Tổng hệ số tối giản của các chất trong phương trình hóa học ở thí nghiệm 3 là 8.
PHẦN III: Câu trắc nghiệm yêu cầu trả lời ngắn.
Thí sinh trả lời từ câu 1 đến câu 6.
Câu 1. Ở trạng thái cơ bản, cấu hình electron lớp ngoài cùng của nguyên tử X là $4s^1$. Số hiệu nguyên tử của nguyên tố X là bao nhiêu?
Câu 2. Cho một số phương pháp bảo vệ kim loại khỏi bị ăn mòn:
(1) Cách li kim loại với môi trường xung quanh.
(2) Dùng hợp kim chống gỉ.
(3) Dùng chất kim hãm.
(4) Ngâm kim loại trong $H_2O$.
(5) Dùng phương pháp điện hóa.
Liệt kê các phương pháp đúng theo dãy số thứ tự tăng dần (Ví dụ: 1345, 124,…).
Câu 3. Cho các kim loại Al, Mg, Fe, Cu lần lượt tác dụng với lượng dư mỗi dung dịch chứa lần lượt ion $Fe^{3+}$, $Cu^{2+}$, $Ag^+$. Có bao nhiêu cặp phản ứng xảy ra tạo thành sản phẩm là kim loại?
Câu 4. Trong tinh thể NaCl, các ion trái dấu tiếp xúc và sắp xếp kề nhau như mô hình sau đây.
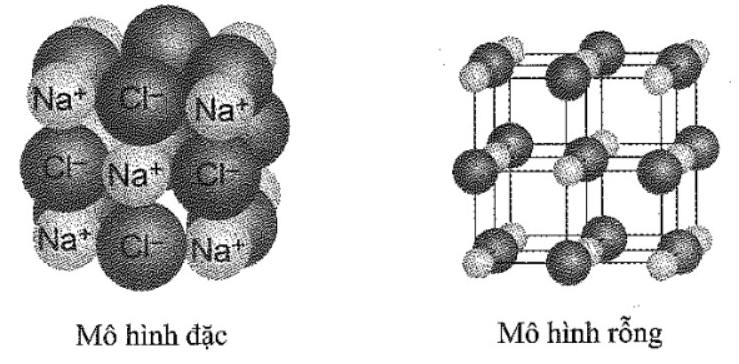
Biết chiều dài cạnh của hình lập phương ô mô hình rồng là a = 564 pm và bán kính ion $Cl^-$ là 182 pm. Bán kính ion $Na^+$ là bao nhiêu pm? (Làm tròn kết quả đến phần nguyên).
Câu 5. Tại SEA Games lần thứ 32, đoàn thể thao Việt Nam đã xuất sắc hoàn thành kỳ Đại hội ở vị trí Nhất toàn đoàn trên bảng xếp hạng với 136 huy chương vàng trong tổng số 359 huy chương. Thực tế, những tấm huy chương vàng không phải được làm từ vàng nguyên chất mà trong thành phần có cả vàng, bạc và đồng. Một mẫu vật liệu làm huy chương vàng nặng 5,000 gam được cho vào dung dịch $HNO_3$ đặc, nóng (lấy dư), phần chất rắn không tan có thể được lọc loại bỏ, để lại dung dịch chứa các muối cần, cô đặc để lọc trong 0,667 gam. Tiếp tục cho thêm HCl vào dung dịch sau khi lọc, thu được tối đa 6,144 gam kết tủa. Khối lượng đồng có trong vật liệu làm huy chương vàng là bao nhiêu gam (làm tròn kết quả đến hàng phần trăm)?
Câu 6. Cho m gam hỗn hợp X gồm Zn và Fe vào dung dịch $CuSO_4$, sau một thời gian thu được 1,02m gam chất rắn Y. Cho toàn bộ Y vào dung dịch $H_2SO_4$ loãng, dư tới khi phản ứng xảy ra hoàn toàn, thu được khí $H_2$ và còn lại 0,856m gam kim loại. Tính phần trăm khối lượng của Z trong m gam hỗn hợp X ban đầu (làm tròn kết quả đến hàng phần mười)?

ThS. Lê Thị Mai Nhi
(Người kiểm duyệt, ra đề)
Chức vụ: Trưởng ban biên soạn môn Hoá Học THPT
Trình độ: Thạc sĩ Hóa học, Chứng chỉ hạng II, Chứng chỉ STEM, Ngoại ngữ B1
Kinh nghiệm: 10+ năm kinh nghiệm tại Trường THPT Chuyên Nguyễn Huệ

.jpg?alt=media&token=949b785a-b067-43aa-bdee-4239c5db8e8d)